
- 25 Фев
- 2026
От эмбриогенеза к нейродегенерации: интервью о современных исследованиях в эпигенетике
Можно ли «переписать» ДНК, чтобы человек рождался полностью здоровым? Об этом и многом другом мы поговорили с научным сотрудником Саарландского университета Константином Лепиховым.
Можно ли изменить судьбу клетки, не переписывая ДНК? На этот вопрос отвечает научный сотрудник Саарландского университета, доктор Константин Лепихов, исследующий механизмы, которые управляют нашим геномом тише и тоньше, чем кажется.
«Казнить нельзя помиловать». Всё решает запятая. Представьте, что геном — это подробная инструкция. В ней уже заложен весь сценарий развития организма. Эпигенетика при этом работает как система пометок на полях. Сам текст остаётся прежним, но именно эти пометки определяют, какие фрагменты будут прочитаны активно, а какие — пассивно. ДНК остаётся неизменной. Меняется способ её чтения. В каждой клетке организма — один и тот же генетический код, но нейрон и клетка кожи живут по разным сценариям. Всё решает регуляция: какие гены активны, какие «молчат», насколько интенсивно и в какой момент.
Эта тонкая настройка лежит в основе самой жизни — от эмбрионального развития до работы взрослого организма. Эпигенетические механизмы определяют, какой ген должен включиться здесь и сейчас, а какой — остаться в тени.
 Можно ли «переписать» ДНК, чтобы человек рождался полностью здоровым? Доктор Лепихов отвечает на этот вопрос следующим образом:
Можно ли «переписать» ДНК, чтобы человек рождался полностью здоровым? Доктор Лепихов отвечает на этот вопрос следующим образом:
«Переписывать ничего не нужно. Речь идёт не о замене текста, а об управлении им. В онкологии такие подходы уже применяются. Например, препарат Децитабин работает именно на уровне эпигенетических изменений, влияя на активность генов, связанных с развитием опухолей».
Но вмешательство требует предельной точности. Невозможно просто «включить» или «выключить» ген — важно понимать контекст: ткань, стадию развития, взаимодействие с другими механизмами. Ошибка может привести к противоположному результату.
В центре исследований Лепихова — метилирование ДНК и работа TET-диоксигеназ, ферментов, которые управляют этим процессом. Их активность способна определить судьбу стволовой клетки — той самой клетки, которая потенциально может стать любой тканью организма.
В лаборатории изучают, как эти механизмы направляют развитие по нейрональной линии — как формируются будущие нервные клетки на ранних стадиях эмбриогенеза.
Сегодня фокус работы расширяется. К исследованиям эмбрионального развития добавлены нейродегенеративные заболевания, такие как Болезнь Паркинсона и Болезнь Альцгеймера. Гипотеза в том, что при этих патологиях может «сбиваться» тонкая эпигенетическая настройка: гены начинают работать не вовремя или, наоборот, замолкают, когда должны быть активны.
Пока это фундаментальная наука. Исследования ведутся на животных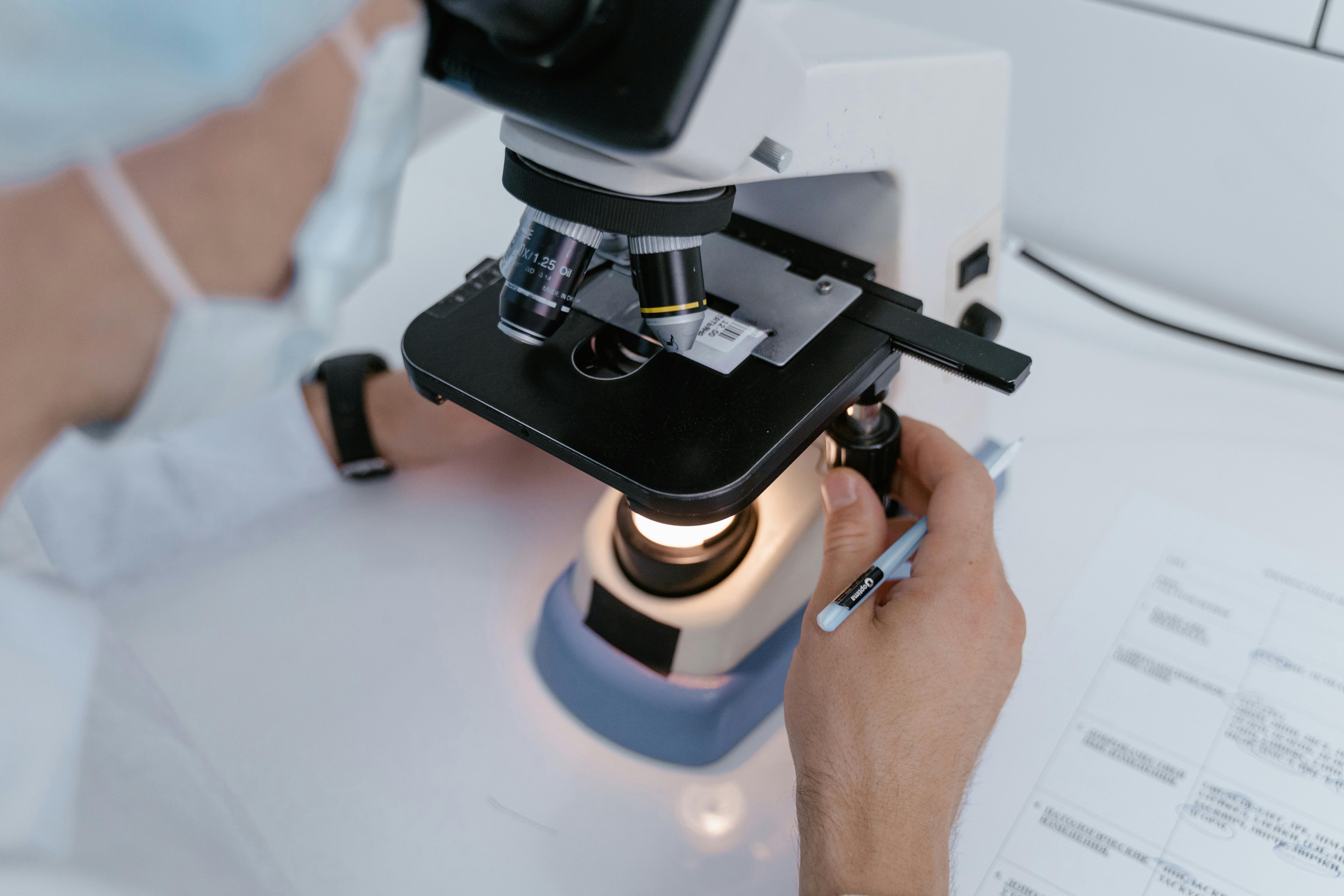 моделях, шаг за шагом выстраивается понимание процессов. Быстрых выводов здесь не делают.
моделях, шаг за шагом выстраивается понимание процессов. Быстрых выводов здесь не делают.
История науки показывает, что прорывы редко бывают запланированными. Когда-то технология CRISPR-Cas9 изучалась как часть бактериального иммунитета. Сегодня это один из ключевых инструментов редактирования генома. Путь от открытия до клиники может занять годы, но начинается он всегда с фундаментальных исследований.
В конце разговора Лепихов возвращается к своей метафоре.
Генетический текст остаётся тем же. Но от того, как он прочитан, зависит развитие тканей, здоровье организма и будущее медицины.
Иногда, чтобы изменить ход истории, не нужно переписывать книгу. Достаточно правильно поставить запятую…
«Казнить нельзя помиловать». Всё решает запятая. Представьте, что геном — это подробная инструкция. В ней уже заложен весь сценарий развития организма. Эпигенетика при этом работает как система пометок на полях. Сам текст остаётся прежним, но именно эти пометки определяют, какие фрагменты будут прочитаны активно, а какие — пассивно. ДНК остаётся неизменной. Меняется способ её чтения. В каждой клетке организма — один и тот же генетический код, но нейрон и клетка кожи живут по разным сценариям. Всё решает регуляция: какие гены активны, какие «молчат», насколько интенсивно и в какой момент.
Эта тонкая настройка лежит в основе самой жизни — от эмбрионального развития до работы взрослого организма. Эпигенетические механизмы определяют, какой ген должен включиться здесь и сейчас, а какой — остаться в тени.
 Можно ли «переписать» ДНК, чтобы человек рождался полностью здоровым? Доктор Лепихов отвечает на этот вопрос следующим образом:
Можно ли «переписать» ДНК, чтобы человек рождался полностью здоровым? Доктор Лепихов отвечает на этот вопрос следующим образом: «Переписывать ничего не нужно. Речь идёт не о замене текста, а об управлении им. В онкологии такие подходы уже применяются. Например, препарат Децитабин работает именно на уровне эпигенетических изменений, влияя на активность генов, связанных с развитием опухолей».
Но вмешательство требует предельной точности. Невозможно просто «включить» или «выключить» ген — важно понимать контекст: ткань, стадию развития, взаимодействие с другими механизмами. Ошибка может привести к противоположному результату.
В центре исследований Лепихова — метилирование ДНК и работа TET-диоксигеназ, ферментов, которые управляют этим процессом. Их активность способна определить судьбу стволовой клетки — той самой клетки, которая потенциально может стать любой тканью организма.
В лаборатории изучают, как эти механизмы направляют развитие по нейрональной линии — как формируются будущие нервные клетки на ранних стадиях эмбриогенеза.
Сегодня фокус работы расширяется. К исследованиям эмбрионального развития добавлены нейродегенеративные заболевания, такие как Болезнь Паркинсона и Болезнь Альцгеймера. Гипотеза в том, что при этих патологиях может «сбиваться» тонкая эпигенетическая настройка: гены начинают работать не вовремя или, наоборот, замолкают, когда должны быть активны.
Пока это фундаментальная наука. Исследования ведутся на животных
 моделях, шаг за шагом выстраивается понимание процессов. Быстрых выводов здесь не делают.
моделях, шаг за шагом выстраивается понимание процессов. Быстрых выводов здесь не делают.История науки показывает, что прорывы редко бывают запланированными. Когда-то технология CRISPR-Cas9 изучалась как часть бактериального иммунитета. Сегодня это один из ключевых инструментов редактирования генома. Путь от открытия до клиники может занять годы, но начинается он всегда с фундаментальных исследований.
В конце разговора Лепихов возвращается к своей метафоре.
Генетический текст остаётся тем же. Но от того, как он прочитан, зависит развитие тканей, здоровье организма и будущее медицины.
Иногда, чтобы изменить ход истории, не нужно переписывать книгу. Достаточно правильно поставить запятую…
Похожие посты

Неудачи великих ученых
24 Январь, 2025

Наука и биотехнологии: молодой ученый Шушаник Казарян о перс...
26 Февраль, 2025

Великие случайности: открытия, изменившие мир
18 Март, 2025

Как литературные персонажи стали терминами в психологии
16 Июнь, 2025

Почему мы чувствуем чужую боль?
11 Июль, 2025

Наука против морали: пять шокирующих экспериментов
28 Июль, 2025

Синдром самозванца и учёба: как сомнения мешают раскрыть пот...
06 Август, 2025

Максим Замшев: «Цифровые платформы не отменят печатную газет...
22 Сентябрь, 2025

Топ-5 советов: как научиться писать по-настоящему хорошие те...
24 Октябрь, 2025

"Сто лет народной дипломатии": в Москве прошёл Международный...
30 Октябрь, 2025

Роль кальциевой сигнализации в лечении болезни Альцгеймера:...
12 Ноябрь, 2025

Биомедицина на пороге больших перемен: интервью с Ольгой Вла...
28 Ноябрь, 2025

Кофе против старения: как 3–4 чашки в день «омолаживают» кле...
27 Ноябрь, 2025

От надоедливой загадки до секретного оружия ИИ: как на самом...
20 Январь, 2026

Учёные научились «программировать» ДНК
26 Январь, 2026

ChatGPT vs Gemini: технологическая дуэль и новая реальность...
23 Февраль, 2026

Три научных прорыва, которые могут изменить нашу жизнь уже п...
27 Апрель, 2026





